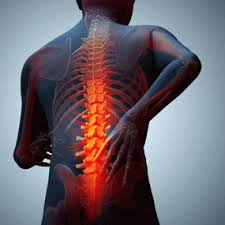
Espondilitis Anquilosante
Consideraciones anatómicas de la columna vertebral: La columna vertebral consta de 24 vértebras y 110 articulaciones. Tiene tres secciones con siete vértebras CERVICALES, doce DORSALES o TORACICAS y cinco LUMBARES. La zona cervical o del cuello es la más móvil. Las vértebras de la sección […]